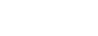Ben je geïnteresseerd in de wereld van wetenschap & technologie en wil je hier graag meer over lezen? Word dan lid van KIJK!
De vruchtbaarheidsbehandeling in-vitrofertilisatie, kortweg ivf genoemd, bestaat veertig jaar in Nederland; op 15 mei 1983 werd de eerste ivf-baby in ons land geboren. KIJK somt drie kunstmatige voortplantingstechnieken op.
1) In-vitrofertilisatie (ivf)
De pionier op het gebied van ivf is Robert Edwards. Eind jaren vijftig begon de in 1925 geboren fysioloog zich te concentreren op de voortplanting, geïnspireerd door onderzoek waarbij in het lab een eicel van een konijn was bevrucht. De Brit besloot zich op de mens te richten en stelde vast hoe menselijke eicellen groeien, welke invloed hormonen op die groei hebben en wanneer een eicel door een zaadcel kan worden bevrucht.
In 1969 slaagde hij erin om een menselijk eitje ‘in de reageerbuis’ te bevruchten, al leidde dat toen niet tot een levensvatbaar embryo. Daarna sloeg Edwards de handen ineen met gynaecoloog Patrick Steptoe, die een techniek had ontwikkeld waarmee volwassen eicellen uit eierstokken konden worden gehaald. Deze samenwerking leidde op 25 juli 1978 tot de geboorte van de eerste reageerbuisbaby: Louise Brown.
Ivf in Nederland
In ons land staan de gynaecoloog Bert Alberda en de bioloog Gerard Zeilmaker bekend als de grondleggers van ivf-behandelingen. Zeilmaker deed in de jaren zeventig al veel onderzoek naar eicelbevruchting in muizen, en wist op een gegeven moment hoe hij een eicel kon bevruchten. Hij kon er alleen niks mee doen, omdat hij als bioloog geen mensen mocht behandelen. De bioloog had nog tevergeefs gynaecologen gevraagd met hem samen te werken, maar die weigerden uit geloofsovertuiging of omdat ze geen heil zagen in het onderzoek.
Toen Alberda als student aan zijn proefschrift werkte, leerde hij Zeilmaker kennen. Na een gesprek stelt hij Alberda voor om samen het onderzoek naar ivf voort te zetten. Dat ging niet zonder slag of stoot; de twee heren hadden met veel weerstand te maken vanuit de medische wereld. Bovendien hield de ethische commissie vervolgstappen, waaronder het terugplaatsen van bevruchte embryo’s in vrouwen, tegen. Toen Nederland werd ingehaald door andere landen op het gebied van ivf-innovatie gaf de commissie eindelijk toestemming. Dat leidde in 1982 tot de eerste ivf-behandeling en, negen maanden later, de eerste ivf-baby in Nederland.
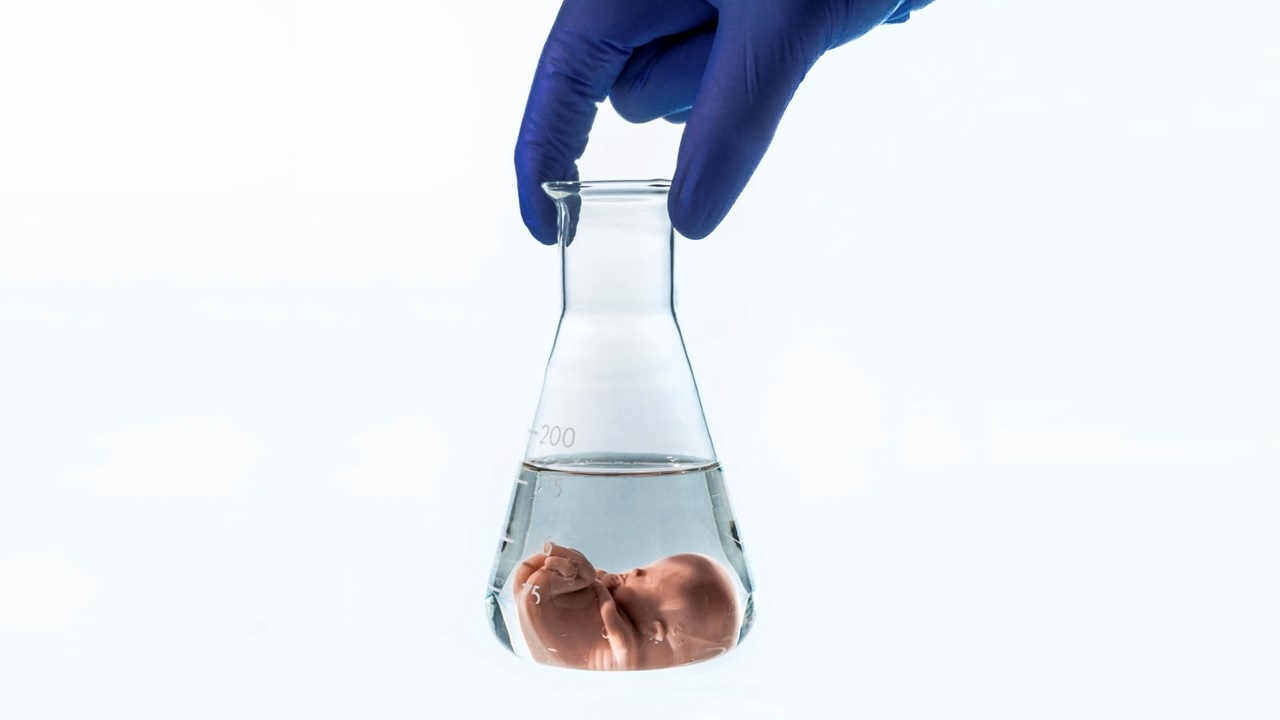
Zo werkt ivf
Een ivf-behandeling begint bij de vrouw, die moet verschillende hormonen geïnjecteerd krijgen die het rijpen van meerdere eicellen bevordert. Middels een echo onderzoekt de arts hoeveel eiblaasjes er rijpen en hoe groot ze zijn. Als die groot genoeg zijn, krijgt de vrouw nog een injectie die voor de laatste rijping van de eicellen zorgt. Daarna worden de rijpe eicellen door middel van een vaginale punctie uit de eierstokken gehaald.
Vervolgens moet de man sperma doneren dat in het lab wordt bewerkt en geschikt gemaakt om bij de eicellen te voegen. Hierna vindt de bevruchting in het lab plaats. Onder de microscoop controleren artsen of er eicellen bevrucht zijn. Daarna kijken ze of er zich een of meer embryo’s ontwikkelen uit de bevruchte eicellen. De meest geschikte embryo’s – soms is één genoeg, andere keren twee – worden geselecteerd voor terugplaatsing in de baarmoeder.
Een garantie op zwangerschap geeft ivf niet. De kans dat het lukt hangt onder andere af van de leeftijd van de vrouw, de duur van het uitblijven van een zwangerschap, en de vraag of de vrouw in kwestie eerdere zwangerschappen heeft gehad. Na drie ivf-behandelingen is de kans op de geboorte van een kind gemiddeld 40 tot 50 procent, meldt Isala op zijn website.
Lees ook:
2) Intracytoplasmatische sperma-injectie (ICSI)
Net als bij ivf vindt de bevruchting bij intracytoplasmatische sperma-injectie (ICSI) buiten het lichaam van de vrouw plaats. Ook de behandeling is min of meer hetzelfde; de vrouw krijgt een hormonencocktail toegediend en de behandelend arts haalt rijpe eicellen weg middels een punctie. Het verschil tussen ivf en ICSI is de manier waarop de bevruchting in het laboratorium gebeurt. Bij ivf brengt een laboratoriummedewerker één eicel samen met ongeveer 100.000 zaadcellen en wacht daarna op spontane bevruchting. Bij ICSI brengt een laborant één enkele zaadcel in één eicel.
Artsen raden ICSI aan als de man een laag aantal beweeglijke spermacellen (‘traag zaad’) heeft of als er na meerdere ivf-pogingen nog geen bevruchting is opgetreden. De kans op het ontstaan van een zwangerschap is met ICSI ongeveer 25 procent per behandeling.
3) In-vitrogametogenese (IVG)
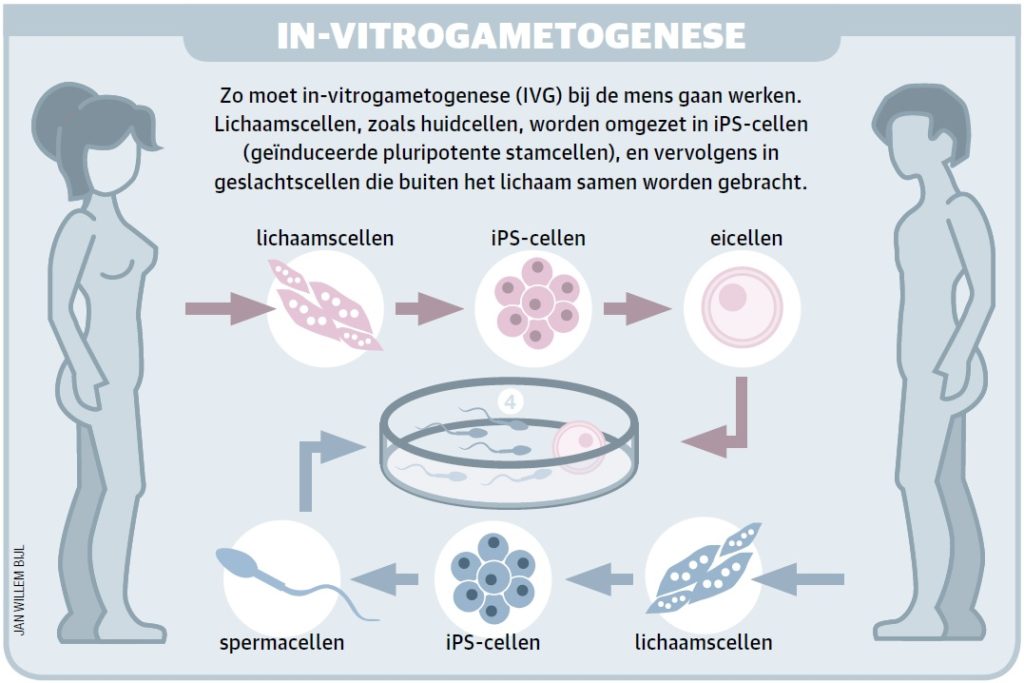
Een redelijk nieuwe techniek is in-vitrogametogenese (IVG). Hierbij worden geslachtscellen (gameten) kunstmatig gemaakt uit stamcellen, cellen die nog in elk celtype kunnen veranderen. Er zijn twee typen stamcellen die kunnen worden gebruikt voor IVG: embryonale stamcellen (ES-cellen) of geïnduceerde pluripotente stamcellen (iPS-cellen), ook wel hergeprogrammeerde lichaamscellen genoemd.
In 2006 ontdekte de Japanner Shinya Yamanaka dat je iPS-cellen kunt maken door cellen van bijvoorbeeld de huid bloot te stellen aan eiwitten die ervoor zorgen dat genen worden afgelezen en omgezet in de gewenste eiwitten. Tegenwoordig is bij mensen van vrijwel ieder celtype, van huidcellen en wangslijmvliescellen tot zenuwcellen en hartspiercellen, aangetoond dat ze in iPS-cellen kunnen worden omgezet. En iPS-cellen kunnen wetenschappers weer veranderen in veel andere typen cellen, waaronder primordiale kiemcellen. Dit zijn de voorlopers van spermacellen en eicellen.
Wangslijmbaby’s?
Verschillende muizenstudies hebben al aangetoond dat er met IVG gezonde pups kunnen worden voortgebracht. Maar wat betekent dat voor onvruchtbare mensenkoppels? Kunnen die straks een speekselmonster bij een lab inleveren, waar specialisten er wangslijmvliescellen uithalen, die omzetten in iPS-cellen, en vervolgens in kunstmatig sperma of eicellen? Zo simpel zal het bij de mens niet zijn. Ten eerste zijn er wel honderden verschillen in voortplanting tussen mens en muis. Een daarvan is dat de menselijke cyclus 28 dagen bedraagt en die van de muis vier dagen. Tot nu toe zijn wetenschappers er bij de mens dan ook niet in geslaagd verder te komen dan het kweken van primordiale kiemcellen (de voorlopers van sperma- en eicellen). Maar door de proeven met de muizen denken sommige wetenschappers dat het wel mogelijk is. En dan hebben we het nog niet eens gehad over de ethische bezwaren van deze behandeling.
Een artikel door drie bio-ethici dat begin 2017 in het tijdschrift Science Translational Medicine verscheen, schetst de gevolgen van IVG voor de toekomstige samenleving. Een positief gevolg is uiteraard dat iedere onvruchtbare persoon met een kinderwens die alsnog kan vervullen.
Maar er zijn ook keerzijdes aan de toename van IVG, zo waarschuwt Glenn Cohen van Harvard Medical School, een van de auteurs van het hierboven genoemde artikel. “Iemand zou ongevraagd lichaamscellen van je kunnen afnemen en daarmee een kind kunnen maken”, vertelt hij. “In het ergste geval kun je naar de hotelkamer gaan waarin bijvoorbeeld Brad Pitt verbleef en daar huidcellen uit het bad halen die je via IVG omzet naar spermacellen waarmee je een vrouw kunt insemineren. Ook zou je kinderen kunnen krijgen van al overleden mensen, voor velen een bizar idee.”
Kortom, er zitten best nog wat haken en ogen aan kunstmatige voorplanting. Maar voor de zekerheid moeten de Brad Pitts van deze wereld in de toekomst misschien hun hotelbad goed uitspoelen.
Tekst: Marysa van den Berg | Laurien Onderwater
Bronnen: KIJK 1/2018, Isala, UMC Utrecht, RTL Nieuws
Beeld: ERWIN WODICKA/123RF